Uue raporti kohaselt võis eksperimentaalne ravi bakteritega võitlevate viirustega aidata kriitilise "superbugi" nakkusega briti teismeliste elu päästa.
Teismelisel, 17-aastasel Isabelle Carnell-Holdawayl on tsüstiline fibroos ja pärast 2017. aastal oma seisundi raviks kopsutransplantatsiooni saamist välja arenenud laialt levinud bakteriaalne infektsioon. (Tsüstiline fibroos on geneetiline seisund, mis põhjustab hingamissüsteemi ja Muud organid ja suurendab kopsuinfektsioonide riski.) Vaatamata ravile antibiootikumidega levivad bakterid tema kirurgilisse haavakohta, maksa ja enam kui 20 nahakohta. Tema prognoos oli sünge - üks arst andis talle CNN-i andmetel ellujäämise võimaluse vähem kui 1%.
Kuid see kõik muutus pärast seda, kui teda raviti kolme spetsiaalselt rünnaku alla sattunud viiruse kokteiliga Mycobacterium abscessus, nakkust põhjustav ohtlik bakter. Kolmest viirusest kaks viidi geneetiliselt läbi, et aidata neil baktereid paremini tappa, tehes Isabelle'i juhtumist esimest korda geneetiliselt muundatud viirusi antibiootikumiresistentsete nakkuste raviks, ütlesid autorid.
Pärast ravi hakkas Isabelle seisund paranema: tema kirurgiline haav paranes järk-järgult, nagu ka muud nakatunud naha piirkonnad, vastavalt 8. mail ajakirjas Nature Medicine avaldatud raportile. Ta hakkas kaalus juurde võtma ja on naasnud kooli, teatas CNN.
Kuid kuidas see teraapia toimib?
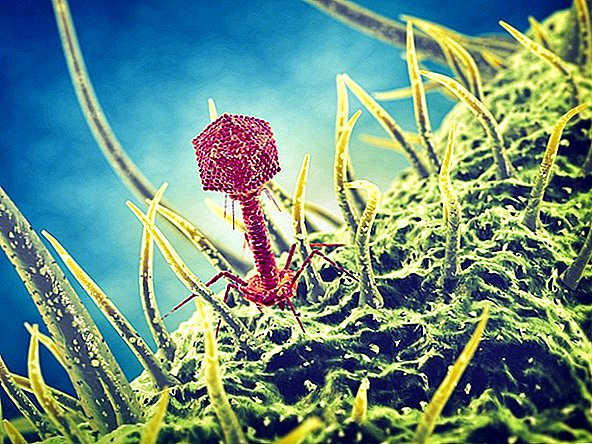
Raviks kasutatakse spetsiaalseid viirusi, mida nimetatakse bakteriofaagideks või lühidalt faage, mis on planeedil kõikjal levinud. Nendel viirustel on üks eripära: nad nakatavad naturaalselt baktereid. Kui nad seda teevad, replitseeruvad viirused bakterirakus ja tapavad selle replikatsiooniprotsessi kaudu bakteri, ütles Pittsburghi ülikooli bioloogiateaduste professor Graham Hatfull.
"Kahe teraga mõõk"
Kuid kui need bakterid tapavad viirused on nii tõhusad, siis miks pole nende kasutamine enam levinud?
Tegelikult on faagid väga spetsiifilised nende nakatatud bakterite suhtes - see tähendab, et antud faag võib nakatada ainult ühte bakteritüve - mis on "kahe teraga mõõk", ütles Hatfull Live Science'ile. Ühest küljest toimivad viirused nagu "juhitavad raketid, et minna mööda väga spetsiifilisi patogeene, millega patsient on nakatunud, ja jätta ülejäänud mikrobioom ja kõik muud bakterid üksi", ütles Hatfull. See tähendab, et faagiteraapial ei ole tavaliselt kõrvaltoimeid. Kuid teisest küljest võivad nad olla nii spetsiifilised, et ühe konkreetse infektsiooniga patsiendil töötav faag ei pruugi töötada sama patsientide puhul, kes on nakatunud sama bakteriliigiga, ütles ta.
Isabelle puhul kammisid teadlased umbes 10 000 faasi, mis olid kureeritud Hatfulli labori poolt, nende jaoks, mis toimiksid tema nakatunud bakteritüve vastu. See hõlmas 10 000 faagi sorteerimist, et vähendada neid umbes 50–100 parimate kandidaatide hulka, ja nende kandidaatide individuaalset läbivaatust nende nakatumisvõime osas M. mädanik, Ütles Hatfull.
Lõppkokkuvõttes leidsid teadlased ainult ühe faagiviiruse, mis suutis baktereid tõhusalt nakatada ja tappa. Nad leidsid veel kaks, mis võivad nakatuda M. mädanik, kuid ei olnud bakterite tapmisel eriti head. Nii et teadlased modifitseerisid neid kahte viirust geneetiliselt, muutes need "vaestest tapjatest ... tõesti headeks tapjateks", ütles Hatfull.
Tulevad meelde kasvava ohu vastu võitlemiseks
Idee kasutada baktereid nakkuste ravimiseks faagi on olnud juba umbes 100 aastat, kuid see unustati antibiootikumide avastamisega suuresti. Antibiootikumiresistentsuse kasvava ohu tõttu on huvi selle piirkonna vastu hakanud kasvama alles viimastel aastakümnetel.
Oluline on märkida, et Isabelle ei ole ikka veel täielikult oma nakkusest ravitud. Ja kuna selles uuringus osales ainult üks patsient, ei saa teadlased kindlalt öelda, kas Isabelle paranemine oli otseselt faagiteraapia tulemus (kuigi tõendite kohaselt oli see nii).
Teadlased ütlesid, et nad loodavad, et uus töö julgustab selles valdkonnas rohkem uurima.
Uus juhtum näitab, et "kui sobitada hea faagikomplekt patsiendi konkreetse infektsiooniga, saame seda infektsiooni tõhusalt kontrollida ... ja selle patsiendi päästa" - ütles Hatfull.
Tulevaste uuringute käigus tuleks uurida selliseid küsimusi nagu seda, milliseid haigusi saaks kõige paremini ravida faagiteraapiaga, milline annus oleks vajalik ja kui kaua ravi seda manustatakse, ütles Hatfull.
Uus töö on vaid väike samm faagiteraapia suures pildis, aga "tohutu samm patsiendi jaoks", ütles Hatfull.












